 Traitement chirurgical des anévrysmes de la circulation antérieure
Traitement chirurgical des anévrysmes de la circulation antérieure
Résumé et mots clé
Toute chirurgie anévrysmale comporte les même temps opératoires, avec à chaque fois les mêmes questions à se poser lors du planning pré-chirurgical. Le premier temps, après la craniotomie, consiste à évoluer dans l’espace sous-arachnoïdien (vallée sylvienne, citerneoptico-carotidienne, etc…) pour accéder à l’anévrysme et aux branches artérielles associées. A ce stade-là, il sera très important de savoir obtenir la détente cérébrale nécessaire à la dissection. Le deuxième temps consiste à identifier le vaisseau porteur de l’anévrysme ainsi que ces branches de division, afin d’en maintenir le contrôle à tous les temps de la dissection. Certains éléments visibles sur l’imagerie pré-opératoire permettront d’ores-et-déjà de s’orienter vers un clampage temporaire, partiel ou total. Le troisième temps représente la dissection de l’anévrysme et la compréhension des rapports du sac et du collet avec les branches artérielles avoisinantes. La pose du clip intervient ensuite, dans un quatrième temps, lorsque la situation est parfaitement comprise et maîtrisée.Enfin, la dernière étape consiste en la validation de l’acte par une ponction du sac permettant de s’assurer de l’exclusion complète de l’anévrysme et une vidéo-angiographie au vert d’indocyanine permettant de valider la perméabilité des différents axes artériels impliqués.C’est selon ce schéma que nous vous proposons cet article portant sur la chirurgie des anévrysmes de la circulation antérieure (péri-calleux exclus).
Mots clé : anévrysme intracrânien, chirurgie, clipping, wrapping
I. Définition et anatomie :
Un anévrysme est défini par la perte de parallélisme des parois artérielles. Il en existe plusieurs types, parmi lesquels le principal rencontré en pathologie intracrânienne est l’anévrysme sacciforme. Le traitement des anévrysmes plus complexes (fusiformes par exemple) n’est pas envisagé dans cet article.Pour les anévrysmes sacciformes, on définit un sac, un collet et un dôme. Le sac peut être multilobé. Enfin, il existe souvent des zones de fragilité sur le sac correspondantà des phlyctènes.Un anévrysme est dit géant lorsque le diamètre maximal de son sac est supérieur ou égal à 25mm.
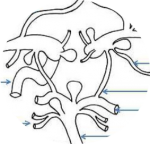
Dans son article sur les anévrysmes, A. L Rhoton 1 décrit 3 « lois » anatomiques régissant la localisation des anévrysmes sacciformes sur le polygone de Willis. La première dit que les anévrysmes se trouvent au niveau d’une bifurcation du vaisseau porteur, soit à la naissance d’une branche collatérale (artère communicante postérieure / artère carotide interne par exemple), soit à la division du tronc principal en ses branches terminales (terminaison carotidienne ou bifurcation sylvienne par exemple). La deuxième dit que les anévrysmes se situent au niveau d’une courbure artérielle, et sur sa face convexe. La troisième, corollaire de la deuxième, dit que le dôme (et en général la phlyctène de rupture) pointe dans la direction qu’aurait eu le sang si la portion artérielle proximale à la courbure avait suivi une ligne droite. Ces 3 lois, basées sur des observations anatomiques, sont en concordance avec les théories rhéologiques expliquant la formation des anévrysmes aux points de turbulences (ou stress) hémodynamiques maximales. La localisation préférentielle des anévrysmes peut être résumée sur le schéma suivant

II. Historique : de l’intervention de Dandy à l’ère de l’endovasculaire
Le 23 mars 1937, le neurochirurgien américain Walter Edward Dandy exclut un anévrysme carotidien par un clip en V posé au collet 2. Son rapport indique qu’il s’agissait d’un patient de 43 ans, alcoolique notoire, se présentant avec une ophtalmoplégie et un ptosis douloureux. Sans demander une angiographie carotidienne, pourtant développée par Moniz dix ans auparavant, Dandy posa le diagnostic d’anévrysme sur le polygone de Willis. Il opta pour une approche qu’il qualifia « d’hypophysaire », et la dissection fut grandement facilitée par l’atrophie cérébrale du patient. L’anévrysme se présentant facilement, avec un collet étroit, un seul clip plat en V suffit à l’exclure complètement de la circulation. Le patient se réveilla sans complication et la paralysie du III régressa rapidement. A partir de cette date, et jusqu’à l’avènement des techniques endovasculaires, le traitement standard d’un anévrysme intracrânien devint son exclusion par un clip au collet. Le deuxième acte fondateur du traitement des anévrysmes intracrâniens fut le développement des coils détachables par Guglielmi en 1991 3. Très rapidement, les techniques endovasculaires entrèrent en compétition avec la technique classique microchirurgicale. En effet, après l’agrément donné par la FDA (Food and Drug Administration) pour les GDC (Gluglielmi Detachable Coils) en 1995, leur utilisation crût de manière exponentielle, si bien qu’un essai randomisé multicentrique international devint indispensable pour établir avec un bon niveau de preuve l’efficacité et la sécurité de ce système comparé au traitement standard microchirurgical, et donc pour déterminer sa place dans la stratégie thérapeutique.Ainsi, l’essai ISAT (International Subarachnoid Aneurysm Trial) permit d’inclure en 5 ans, de 1997 à 2002, 2143 patients sur 16 centres. Il avait pour objectif de comparer l’efficacité et la sécurité du traitement endovasculaire par coïlsversusmicrochirurgie pour les patients souffrant d’HSA par rupture d’anévrysme datant de moins de 28 jours, pour lesquels neurochirurgiens et neuroradiologues avaient convenu sur la base des données angiographiques que les deux traitements étaient envisageables et qu’il existait un doute quant au meilleur traitement à proposer. N’étaient pas inclus les patients jugés trop graves ou trop âgés ou ayant de trop lourds antécédents pour justifier d’un traitement actif de leur rupture d’anévrysme. Il est important de noter que sur les 9559 patients éligibles pour la randomisation, seuls 2143 (22%) furent inclus dans l’étude. Cela signifie que cette cohorte, bien qu’importante, n’était pas représentative de la population globale des patients souffrant d’hémorragie méningée anévrysmale. Ainsi, les patients inclus étaient en relativement bon grade clinique (plus de 85% de WFNS 1 ou 2), la moitié des anévrysmes faisait moins de 5mm et provenaient du complexe cérébral antérieur pour 50% ou de la carotide interne pour 32,5% d’entre eux contre 2,7% provenant de la circulation postérieure. La conclusion après 1 an de suivi après traitement fut une réduction du risque relatif de décès ou de handicap sévère de 22,6% (IC95% 8,9 – 34,2) après traitement par embolisation par coils par rapport au traitement microchirurgical, avec cependant, déjà à 1 an, un bémol sur le taux de récidive hémorragique dans le bras endovasculaire et un doute sur la pérennité de l’effet de ce traitement.L’analyse récente des résultats à 10 ans de suivi (concernant uniquement les patients inclus au Royaume-Uni) montre,quant à elle, une légère supériorité du traitement endovasculaire par rapport au traitement microchirurgical sur la probabilité d’être vivant et indépendant, OR = 1,34 [IC95% 1,07 – 1,67] 6.Cependant, cette étude n’a comparé que le coiling simple tel que pratiqué durant la période d’inclusion (1994 – 2002) au traitement chirurgical. Depuis, de nombreuses techniques endovasculaires ont vu le jour dans le but de traiter les anévrysmes à collet large. Citons le « remodelling » par ballonnet, utilisable en période aiguë de l’HSA, ou l’utilisation de stents et de flow-diverters, nécessitant une couverture par antiagrégation plaquettaire et donc contre-indiqués dans les 10 jours suivant le saignement anévrysmal. Ces techniques, de plus en plus usitées à l’heure actuelle, n’ont pas fait la preuve de leur efficacité et de leur sécurité d’emploi dans une étude prospective randomisée les comparant au traitement microchirurgical. Ainsi, bien que les résultats d’ISAT ne fussent applicables qu’au type de patient inclus dans l’étude et à une embolisation par coïls simples, et non pas à n’importe quel patient admis aux urgences pour anévrysme rompu, la portée des résultats de cette étude dépassa largement le cadre des critères d’inclusion des patients. Ainsi, les techniques endovasculaires, initialement développées pour pallier à l’impossibilité du traitement microchirurgical dans certaines situations, se sont très rapidement, en une décennie, imposées comme le traitement standard et de première intention de la majorité des anévrysmes en France et en Grande-Bretagne. Ceci est illustré par le fait que, en 2011, 85% des anévrysmes ont été traités par voie endovasculaire au Royaume-Uni 6. La situation actuelle, marquée par la suprématie du traitement endovasculaire des anévrysmes a clairement mené à se poser la question suivante : reste-t-il des indications chirurgicales ?
Dans le but de palier à l’absence de représentativité de la cohorte ISAT par rapport à l’ensemble des patients souffrant d’HSA anévrysmale, l’équipe du Barrow Neurological Institute proposa une étude randomisée contrôlée prospective unicentrique (BRAT : Barrow Ruptured Aneurysm Trial) portant sur tous les patients admis pour hémorragie méningée anévrysmale entre 2003 et 2007. Dès leur arrivée aux urgences, 408 patients furent randomisés en 2 bras :exclusion par clip(209)versusembolisation (199) et analysés en intention de traiter 7. Bien que la modeste taille de la cohorte ne permit pas de conclure à une différence significative entre les 2 bras concernant l’objectif principal sur un suivi à 6 ans (nombre de patients décédés ou dépendants soit un mRS >2 comme dans ISAT), les résultats permirent de mettre au clair au moins un point intéressant. Sur 199 patients alloués au traitement endovasculaire, 75 (38%) bénéficièrent en fait d’une chirurgie, contre 4 patients initialement randomisés dans le brasexclusion par clipet finalement embolisés. Cette différence de cross-over (38% coils vers clip) contre 1.9% (clip vers coils) montrait que l’embolisation ne permettait d’apporter une solution adéquate que dans 62% des situations d’anévrysme rompu alors que 98% des situations pouvaient être résolues par la chirurgie.
En conclusion de cette revueportant sur les deux seules études randomisées contrôlées prospectives comparant traitement endovasculaire et chirurgical dans le cas des anévrysmes rompus, il semblerait que le premier soit supérieur au second en terme de survie sans handicap (mRS < 3) à court terme (à 1 an post-traitement, mais pas à 5 ans et peut-être à 10 ans) dans les cas d’anévrysmes rompus de petite taille et de la circulation antérieure (essentiellement complexe communicant antérieur) chez des patients en bon état clinique, avec un traitement uniquement par coiling simple. Les autres stratégies thérapeutiques (embolisation d’un anévrysme puis évacuation d’un hématome dans les hémorragies cérébro-méningées, « remodelling » par ballonnet, embolisation partielle d’un anévrysme complexe rompu en attendant un deuxième traitement à froid par stenting ou flow-diverter) n’ont pour l’instant pas été comparées au traitement chirurgical. Enfin, l’effet du traitement endovasculaire semble moins pérenne, avec un taux d’occlusioncomplète de l’anévrysme par traitement endovasculaire n’excédant pas 60% dans la littérature, contre plus de 90% pour le traitement chirurgical, aboutissant à un retraitement de l’anévrysme dans 16% et 4% des cas respectivement 7.A la lumière de ces données, nous pensons qu’il n’y a pas d’arguments pour proposer un traitement endovasculaire en première intention à tout patient admis pour rupture d’anévrysme mais que la discussion entre chirurgie et embolisation doit avoir lieu pour chaque situation clinique. A fortiori, le traitement chirurgical doit garder toute sa place dans les cas de :
- Sujets jeunes présentant donc un risque cumulatif plus élevé de recanalisation en cas de traitement endovasculaire
- Architecture défavorable à un traitement par coiling simple : collet large, branches naissant au collet : chirurgie en première intention selon les données de l’angioTDM ou en seconde intention après échec d’embolisation
- Localisations particulières : anévrysmes sylviens car souvent d’architecture complexe, anévrysmes de l’artère communicante postérieure (20% de recanalisation dans ISAT)
- Situations cliniques particulières : hémorragie cérébro-méningée avec hématome réalisant un effet de masse,et l’anévrysme de l’artère communicante postérieure responsable d’uneparalysie oculomotrice demeilleur pronosticde récupération fonctionnelle après traitement chirurgical 8,9.
- Aucune donnée prospective comparative randomisée n’étant disponible dans les cas des anévrysmes asymptomatiques à l’heure actuelle, le traitement, s’il est indiqué, sera discuté en réunion de concertation pluridisciplinaire (neurochirurgiens et neuroradiologues) et les mêmes caractéristiques (âge du patient, comorbidités,angio-architecture anévrysmale) seront prises en compte.
 Encyclopædia Neurochirurgica
Encyclopædia Neurochirurgica

